Nga cấp phép sử dụng trong nước vaccine COVID-19 thứ 3
Nga vừa cấp phép sử dụng loại vaccine ngừa COVID-19 có tên CoviVac do Trung tâm Chumakov phát triển và sản xuất.
Đây là loại vaccine thứ 3 được Nga cấp phép sử dụng trong nước, sau 2 loại vaccine của Viện Gamaleya và Viện Vector.
Thủ tướng Nga Mikhail Mishustin đã công bố thông tin này trên truyền hình. Ông bày tỏ sự tự hào khi Nga là quốc gia duy nhất hiện sở hữu 3 loại vaccine ngừa COVID-19.
Không giống như vaccine Sputnik V có cơ chế sử dụng virus vô hại đưa protein của SARS-CoV-2 vào tế bào người, giúp kích thích phản ứng miễn dịch, CoviVac là loại vaccine hàm chứa toàn thành phần virus, qua đó được đánh giá là loại vaccine có khả năng bảo vệ người dùng trước mọi biến thể của virus SARS-CoV-2. Hiện Nga chưa triển khai tiêm chủng loại vaccine này.
Đến nay, Nga đã sản xuất tổng cộng 11,1 triệu liều vaccine, trong đó có 7,9 triệu liều đã được phân phối cho các chương trình tiêm chủng nội địa.
Cũng liên quan đến việc sản xuất vaccine COVID-19, cuối tuần qua, hãng Johnson & Johnson (Mỹ) đã trình Tổ chức Y tế Thế giới (WHO) hồ sơ xin cấp phép sử dụng khẩn cấp cho vaccine ngừa COVID-19 do hãng sản xuất.
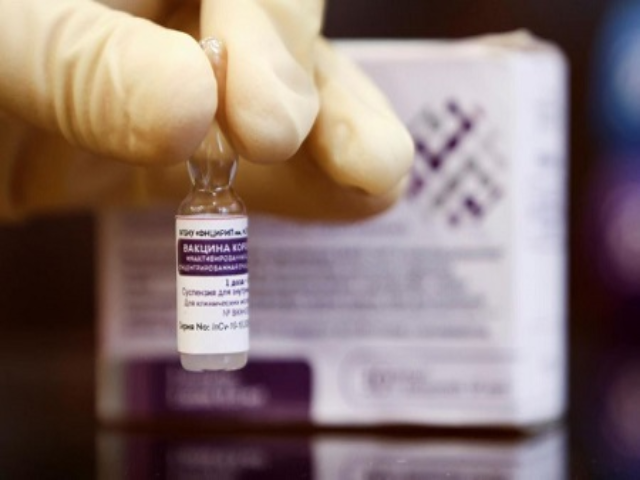 Vaccine CoviVac của Nga.
Vaccine CoviVac của Nga.
Johnson & Johnson cho biết đây là điều kiện tiên quyết để có thể cung cấp vaccine cho cơ chế phân phối vaccine công bằng COVAX do WHO khởi xướng cùng với Liên minh Vaccine toàn cầu (Gavi) nhằm hỗ trợ vaccine cho các nước nghèo và có thu nhập trung bình.
Vaccine của Johnson & Johnson là loại chỉ tiêm một liều duy nhất và có thể bảo quản ở nhiệt độ lạnh bình thường. Đây chính là một ưu điểm lớn đối với các nước có cơ sở hạ tầng y tế tương đối yếu kém.
Hiện vaccine của hãng đang được Cơ quan Quản lý dược phẩm và thực phẩm của Mỹ (FDA) đánh giá và dự kiến đưa ra quyết định vào tuần tới. Kết quả thử nghiệm cho thấy vaccine có hiệu quả tới 66% đối với nhiều biến thể khác nhau của virus SARS-CoV-2.
Tuy nhiên, mức độ bảo vệ của vaccine không giống nhau ở các nước, cụ thể như 72% tại Mỹ, 66% tại Mỹ Latin và 57% tại Nam Phi. Công ty Johnson & Johnson cho biết dữ liệu trình WHO bao gồm cả kết quả của cuộc thử nghiệm giai đoạn cuối.
Trong một diễn biến khác, báo Nikkei ngày 21/2 đưa tin, Tập đoàn Fujifilm của Nhật Bản sẽ tái khởi động thử nghiệm lâm sàng thuốc Avigan trong điều trị COVID-19. 270 bệnh nhân sẽ tham gia cuộc thử nghiệm lần này và Fujifilm đặt mục tiêu cho Avigan sẽ được cấp phép trong tháng 10 năm nay.
Đại diện của Fujifilm hiện chưa đưa ra bình luận gì về thông tin trên. Trước đó, quá trình cấp phép sử dụng thuốc Avigan trong điều trị COVID-19 tại Nhật Bản đã bị trì hoãn sau khi giới chức y tế nước này hồi tháng 12/2020 cho rằng các dữ liệu thử nghiệm không thuyết phục.
Nhật Bản đã phê chuẩn thuốc Avigan, thường được biết dưới cái tên Favipiravir, để sử dụng cho chữa bệnh cúm khẩn cấp. Tuy nhiên, vẫn còn những lo ngại khi Avigan gây dị tật bẩm sinh ở các loài vật thí nghiệm và chưa thể hiện được hiệu quả đối với COVID-19. Chính phủ Nhật Bản đã yêu cầu Fujifilm tăng gấp 3 lượng dự trữ quốc gia thuốc Avigan. Hiện Avigan đã được phê chuẩn để điều trị COVID-19 tại Nga, Ấn Độ và Indonesia.
Trong khi đó, Nhật Bản đã nhận lô vaccine ngừa COVID-19 thứ hai từ hãng dược phẩm Pfizer (Mỹ) để tiếp tục tiêm chủng cho một số nhân viên y tế trong giai đoạn đầu tiên của chiến dịch. Khoảng 450.000 liều vaccine đã đến thủ đô Tokyo của Nhật Bản sau khi Liên minh châu Âu (EU) "bật đèn xanh" cho việc xuất khẩu vaccine.
(Theo Báo điện tử Chính phủ)





















